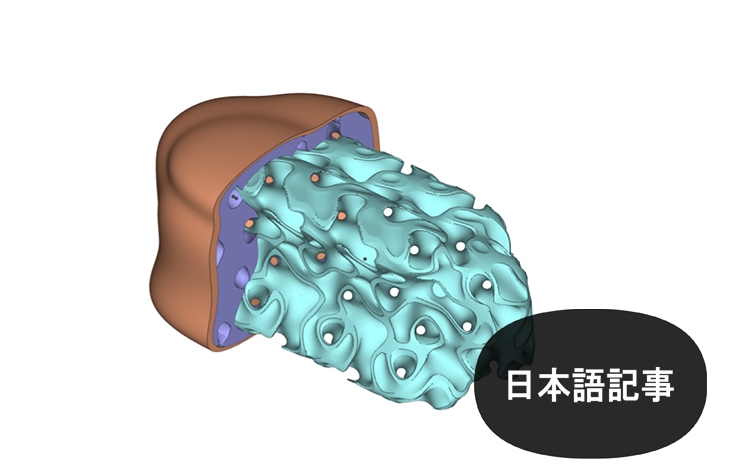
nTop Platformのようなソフトウェアソリューションにより、エンジニアは生物学的に適切でオッセオインテグレーションに最適化された医療用インプラントを設計することができます。
整形外科のインプラントコミュニティでは、自社の技術が骨の内植を促進する(または骨成長の可能性につながる)と主張し、多くの企業がそれぞれの技術の利点を宣伝しています。
しばしば-必ずではありませんが-これらの主張を裏付ける臨床的証拠は、チタンは骨の成長環境を促進させるという、よく繰り返し主張されてきた事実以外にはほとんどありません。
これは特に、チタンをプラズマ溶射した表面や、基質のポロシティがない酸エッチングされた表面の場合によくみられます。
これらは初期の駆出抵抗のための表面を生み出し(移植後のケージの移動を防ぎます)、骨が成長するための表面を提供するかもしれませんが、最良の固定と長期間の成果を提供するための長期の内植をもたらすことはほとんどありません。
優れた多孔質構造を構成するものを評価するために、多くの研究が行われています。
骨組織工学構築物の「理想的な」微細構造は、セラミックベースの骨代替物が評価された1990年代に初めて定義されました。
当時、理想的な細孔径は0.30mmから0.50mmの間のどこかであることが立証されました。
また、0.100mm以下の細孔径では、適切な骨及び血管伝導性に必要な内植空間が得られないことが確認されました。(Galois L, Mainard D. Bone ingrowth into two porous ceramics with different pore sizes: An experimental study. Acta Orthop Belg 2004;70:598–603)
パラメータ化実験によって優れたラティスで構成された物のさらなる改良が引き続き行われ、最終的には、細孔および支柱の大きさに関する長年にわたる信念のいくつかに挑戦した最近の研究(Wild M et al. Osteoconductive Lattice Microarchitecture for Optimized Bone Regeneration. 3D Printing and Additive Manufacturing, Vol. 6, No. 1, 2019.)で、最適な細孔径は0.80mmに近い傾向にあることがわかりました。
そして、続けられる研究によって業界は共通の細孔/支柱のサイズの採用に向かっていますが、さらなる課題が残っており、依然として詳細に検討する必要があります。
- ラティス構造の表面形態 - マクロおよびミクロトポグラフィー
- 最適な初期付着と長期増殖のための、ラティスの型と形状操作
- 最適な細孔/支柱サイズと構造のマクロ剛性の間の相関 - 応力遮蔽および隣接する生物学的問題の防止
- 計算法による力学特性の操作(機能的ラティスのグレーディング、トポロジーオプティマイゼーション等)
こういった種類の問題は、次世代の整形外科インプラントにつながるような構造を構築するための多くのソフトウェアツールに課題を生み出します。
さらに、SLM(selective laser melting)マシンが進歩するにつれて、これらの複雑な構造の製造はますます現実的になりつつあります - 現在では、0.100mm(0.004インチ)以下の支柱サイズや最小0.080mm(0.003インチ)程度のものを解決できるマシンがあります。
nTop Platformは、これらの工学的課題の解決に役立つ次世代ソフトウェアであり、高度なラティス機能操作を可能にする強力なツールを提供しています。
ラティス構造を機能的にグレーディングすることは難しい問題ですが、nTop Platformの様々な能力を用いることにより、設計エンジニアはTPMSラティスを取得し、傾斜構造にあわせてグレーディングできます。
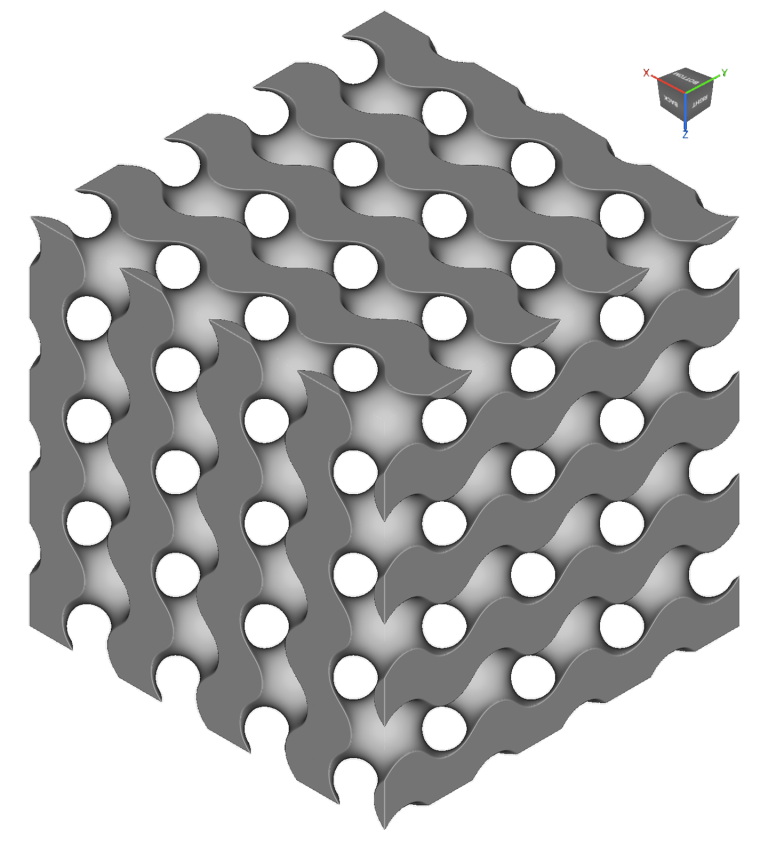

この機能は線形リマッピングまでの話ではありません。それどころか、どんなジオメトリ表現でも、どんな複雑なパラメトリック方程式でも、それぞれの軸で変化させることができます。

また、これは単に軸のみを介したリマッピングに限定されるわけではありません。
複雑なモデルは、パラメータまたはトポロジーオプティマイゼーションを介して生成でき、複雑さにかかわらず、構造を機能的にシームレスにグレーディングするために使用できます。
この機能を示す以下の画像を参照してください。

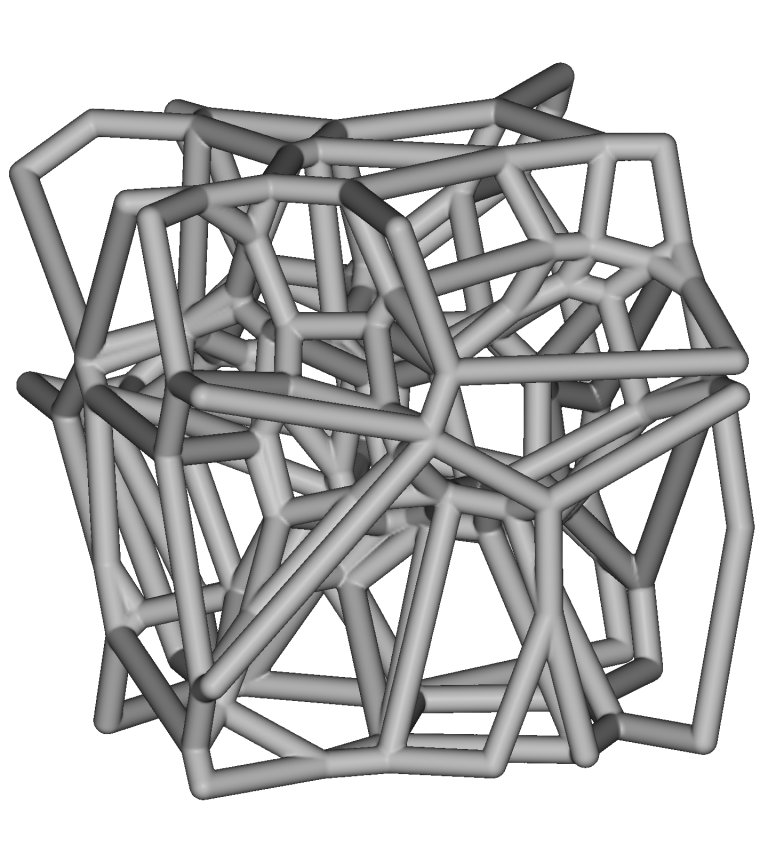
上記の入力を使用すると、ボロノイラティス入力でボリュームラティスをシームレスに厚くさせることができます。
パラメータ化を行えば、厚みの量を正確にコントロールすることができます。
この場合、ボロノイラティス材料が存在する場合、最終ラティス厚はより大きくなります。
まず、ボリュームラティスを設定する際にも同じ原理を適用することができます。細胞のポイント間隔は、考案され適用できるあらゆる表現を介してランプ化することができます。

nTop Platformの機能を使えば、明確な移行点がなくても複雑なラティスをシームレスに互いに変換することができます。
これは、一つの”ずれた”弱点に苦しむことのない構造をもたらします。
2つのまったく異なるマクロ形状間のこのタイプの構造生成は、今まさに現実となりつつある計算上の課題です。
前述したように、このような構造をつくるツールはすでに存在しています。
生物学的利益をもたらす支柱・細孔サイズを得られるだけでなく、構造的要素を操作する自由を持つことで、真の直交異方性特性の複雑な操作が可能となります。
これはさらに、エンジニアが、骨の内植が構築物のマクロ剛性をどのように変化させるか、生物学的最適化に関して長期的利益をもたらすラティス要素をどのように作り出すかを評価するのに役立ちます。
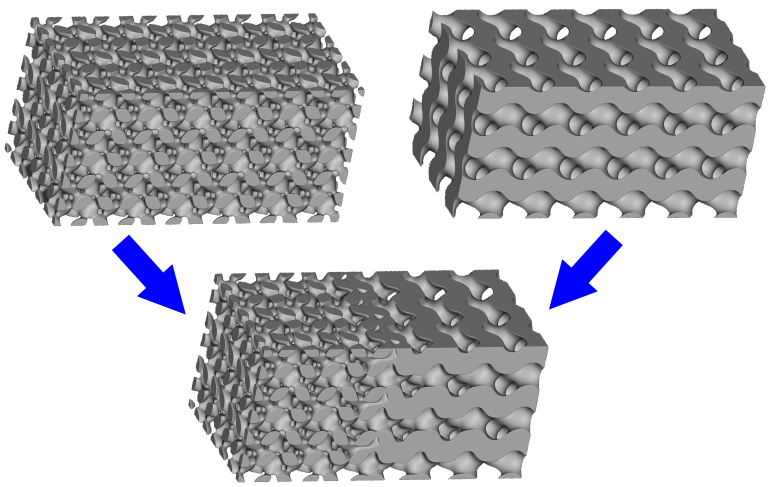
これまでのように、混合要素の操作は線形入力には結合していません。オブジェクトは、複雑な構造または原始的なモデルを用いて混合することができます。
同一の2つのTPMSラティスを斜方球体(水平方向に伸ばした球体)を用いて混合する下記の画像を参照してください。
球体が存在するところでは、細胞はジャイロイドTPMS構造であり、設計は球体から明らかな転移点のないLidinoid細胞構造へと移行します。
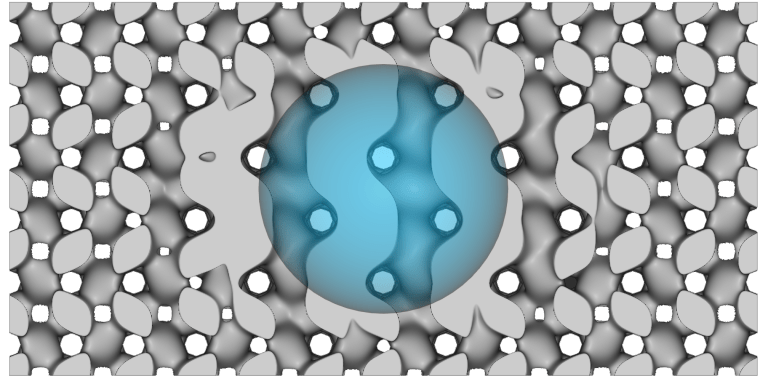
これらのツールは、複雑なラティス形状を外部の固形形状に移行させ、骨構造の生物学的模倣(皮質および骨梁要素)およびそれらの間のシームレスな有機的移行をシミュレートするために使用することができます。
この種の内部および外部構造の制御、ならびに移行要素の個別制御は、インプラント開発者にマクロおよびミクロレベルで構造特性を変化させる能力を与えるのに役立ちます。
また、骨が統合されるにつれて構造がどのように変化するのかを理解するのに役立つとともに、特定の内植因子をもつインプラントを設計することもできます。

これは、以下に紫色で示すように、ある構造要素から別の構造要素への移フェーズを設定することによってさらに精密化することができ、全く異なる構造タイプから連続的な機械的特性を定義できます。
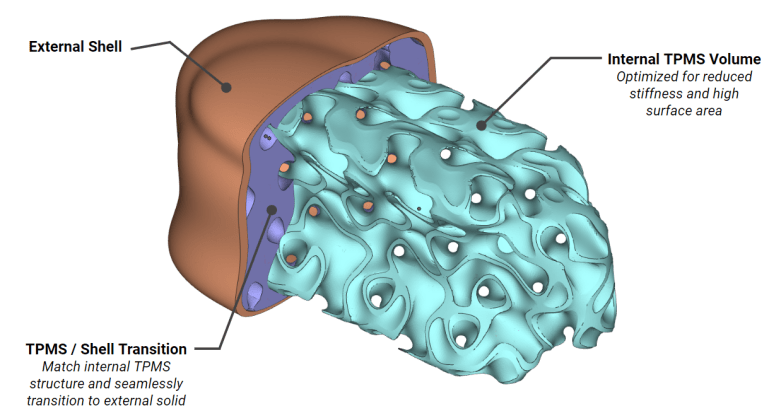
ここに示した例は、生物学的に関連のある構造の設計と構築のためにnTop Platformが提供する利用可能なツールのごく一部です。
Summary
この短い記事では、細孔や支柱の大きさの分析を含め、何が優れた生物学的構造を作るのかに関する研究の歴史をいくつか探ってきました。
また、エンジニアが次世代の高度な構造を構築しようとする際に直面するいくつかの限界、そしてnTop Platformがこれらのツールをどのように提供しているかについても考察しました。
これらのタイプのツールを高度なモデリングのプロフェッショナルの手に置くことは、かつては達成可能と考えられなかった結果を得るために意図的かつ思慮深く設計されたインプラントをさらに強化することに役立つでありましょう。